欧州のCOVID-19症例における血栓症と死亡率
みなさんこんばんは。現役救急医です。今日は久しぶりに論文の紹介です。今年5/13にオンライン発表された'Venous or arterial thrombosis and deaths among COVID-19 cases: a European network cohort study.'(Burn E., Duarte-Salles T. et al., Lancet Infect Dis. 2022)が元ネタです。
(1) 導入
COVID-19は、強い炎症, 血小板活性化, 血管内皮障害, 血流の停滞により血栓症を来す可能性がある。入院COVID-19症例における静脈血栓塞栓症のリスクを評価した研究は複数あり、最近のsystematic review・meta-analysisでは100件以上の研究が特定されている。しかし、こうした研究の大半は比較的小規模であり, 環境・研究デザイン・転帰(outcome)の定義が顕著に異なっている。特異的な超音波検査screeningを用いない臨床研究では、COVID-19入院症例における静脈血栓塞栓症の有病率は0~37%だった。動脈血栓塞栓症に関する臨床研究でも、COVID-19入院症例における動脈血栓塞栓症の有病率は1~18%と推計されている。
今日に至るまで、COVID-19患者の血栓塞栓症の臨床研究は、入院患者における発症だけに注目しているものであった。また、予後や健康関連転帰への血栓症の影響も詳細が記述されていない。血栓塞栓症の有病率がICUに入院した患者で高いことが分かっているものの、発症時期や, 転帰悪化との関連は十分に分かっていない。
高齢・男性・高血圧・糖尿病・肥満といった因子がCOVID-19の入院・死亡リスク上昇と関連している。また、こうした因子が一般集団において血栓塞栓症のリスクを上昇させることが既に示されている。患者の特性と, COVID-19患者における血栓塞栓症のリスクの間の関連性はまだ不明である。
医療記録から日常的に収集したデータから構成される研究コホートは、特に外来・入院COVID-19症例双方をカバーし, また患者側因子と転帰の関連を記述するのに十分なサンプルサイズを確保するに足るデータが収集できた場合、COVID-19における血栓塞栓症の記述に有用となりうる。この研究では、1) COVID-19患者の静脈・動脈血栓塞栓症の発症率と死亡率を要約し, 2) 患者側因子と血栓塞栓症のリスクの間の関連性を記述し, そして 3) 静脈・動脈血栓塞栓症と健康関連転帰の間の関連性を評価するために、欧州各地からのデータを統合させた。
(2) 方法
① Study Designと参加者について
この研究は欧州各地の日常的に収集した医療記録を用いたnetworkコホート研究である。解析に用いられた医療記録は、ドイツ, オランダ, スペイン, 英国由来のものだった。用いられた各国のデータベースの詳細は以下の通り。
- ドイツ・・・IQVIA Disease Analyzer(DA): 一般開業医("general practitioners"), 外来診療を行う専門医("specialists practicing in ambulatory care settings")が使用している患者管理ソフトウェアからのデータを収集。
- イタリア・・・IQVIA Longitudinal Patient Database(LPD): 一般開業医の使用するソフトウェアから、匿名化された患者医療記録を収集。
- オランダ・・・Integrated Primary Care Information(IPCI)データベース: 一般開業医が登録した患者の電子医療記録のデータを収集。
- 英国・・・Clinical Practice Research Datalink(CPRD) Autumデータベース: 一般開業医のデータを使用。
- スペイン・・・System for Reserch in Primary Care(SIDIAP)は同国カタルーニャ州の人口約80%をカバーする、一般開業医医療記録のデータベース("primary care records databese")である。これを、入院中に登録された診断名・行われた処置を記録したConjunto Minimo de Datos Basicos al Alta Hospitala(CMBD-AH)というデータベースとリンクさせた。
Primary analysis(主要解析)のために2つのコホートが作られた。
1) 第1コホート: COVID-19と診断された or RT-PCR検査でSARS-CoV-2陽性と診断された人で構成されるコホート。このコホートに属する各患者の"the index date"(=臨床研究の解析対象となった期日?)は、最初にCOVID-19と診断, ないし RT-PCRで陽性 のいずれかになった期日であった。
2) 第2コホート: SIDIAP CMBD-AHのみでカバーしているCOVID-19入院患者のコホート。このコホートの"index date"は入院した期日だった。
主要解析において、患者はindex dateより前に少なくとも1年間の経過観察を有している必要があった。
欧州のCOVID-19第1波において特に検査・診断方法・データ収集に差があったため、ここでは2020年4/1以降がindex dateである患者の結果を報告する。この臨床研究の参加登録の終了日("cut-odd dates")は2021年早期で, データベースにより差があった。
② 転帰(outcome)について
主要転帰評価項目("primary study outcome")は、index dateから90日間における 1) 静脈血栓塞栓症(venous thromboembolic events; 以下、VTEと略する), 2) 動脈血栓塞栓症(arterial thromboembolic ebents; 以下、ATEと略する), 3) 死亡, であった。死亡はIQVIA DA以外のデータベース全てで検出可能だった。
患者の人口統計学的データ, 既往歴, 医薬品使用歴が要約された。ここで既往歴(基礎疾患)は以下のものを指す。
- 自己免疫疾患
- 抗リン脂質抗体症候群
- 血友病
- 喘息
- 心房細動
- 悪性新生物(≒癌, 悪性腫瘍)
- 糖尿病
- 肥満
- 心臓病
- 高血圧
- 腎疾患
- 慢性閉塞性肺疾患
- 認知症
対象となった医薬品は、
であった。他に喫煙歴を評価した。
③ 統計学的解析
Outcomeの90日間累積発症率を、患者全体, 及び 年齢や性別で分類して推計した。ドイツのIQVIA DA(死亡に関するデータの信頼性に乏しい)では、Kaplan-Meier法という手法で累積発症率を推計した。死亡リスクの推計には、DA以外の4個のデータベースを用いて累積発生率を求めた。
事前に設定した重要な変量(=既往歴/併存疾患, 医薬品使用歴のこと?)とVTE・ATE・死亡リスクとの関連性を記述する為に、原因特異的Coxモデルという方法が用いられた。年齢とoutcomeの関連性は、性別により分類して検証した。また性別との関連性は、年齢により調整したモデルを使用して推計した。最後に、併存疾患 or 医薬品とoutomeの関連性は、未調整モデル・年齢調整モデル・性別調整モデルで推計した。
VTE・ATEのCOVID-19 outcomeへの影響は、'multistate model'という手法を用いて検証した。Multistate modelとは、被験者の症状進行を考慮することを可能としており, 以前もカタルーニャ州のCOVID-19第1波時の患者転帰を記述するために開発されていた。同様のモデルを、COVID-19無し・一般集団から始まり, 外来でCOVID-19と診断・COVID-19で入院・死亡のいずれにも進行しうる被験者に対して用いた。このモデルを、SIDIAP CMBD-HA由来のデータへ使用した。開始集団("starting population")は、SIDIAP CMBD-HAに属し, 2020年4/1時点で既往歴が少なくとも1年間はデータベースに記録されており, COVID-19既往 or SARS-VoV-2陽性歴がなく, かつ その前の1年間にVTE or ATEの既往が無い 患者だった。次に、以下のような時間依存性曝露について, VTE・ATEで個別に評価した: 1) 外来でCOVID-19 or PCR陽性と診断されてから入院するまで, 2) 外来でCOVID-19 or PCR陽性と診断されてから死亡するまで, 3) 入院してから死亡するまで。
(3) 結果
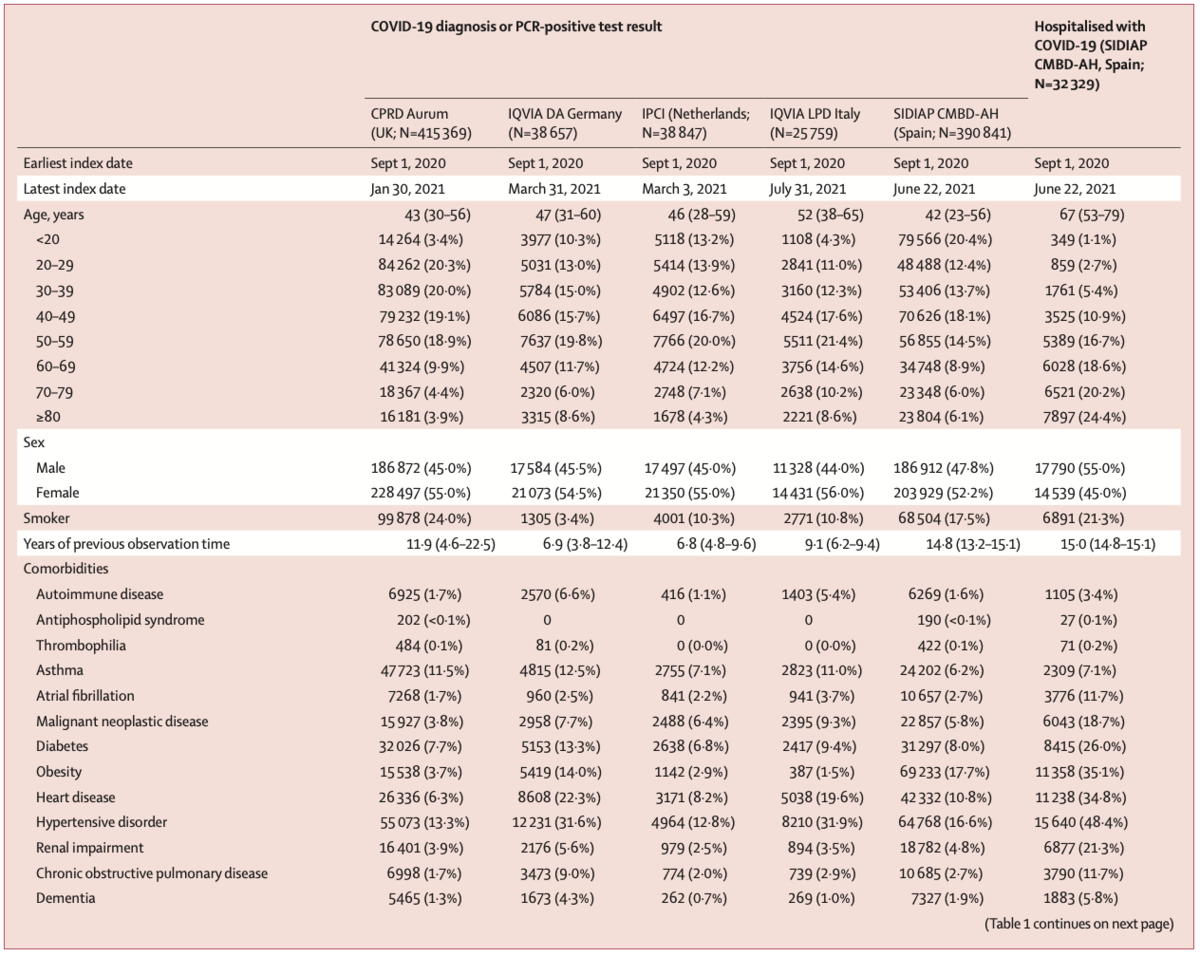
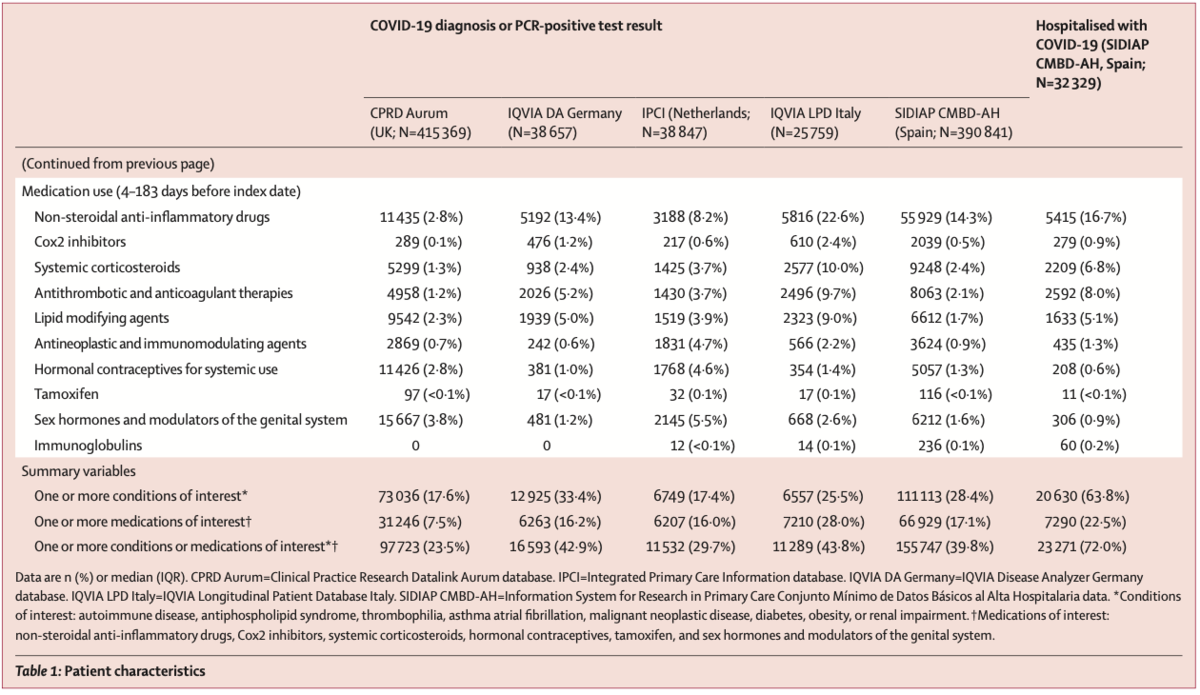
全体として、index dateが2020年4/1以降の患者909,473名が対象となった。これに加えて、SIDIP CMBD-AHからは32,329名のCOVID-19入院患者コホートが特定された。COVID-19と診断 or PCRで陽性となった患者の年齢中央値の範囲は、41歳(SIDIAP CMBD-AH)から52歳(LPD)であった。全てのデータベースにて、COVID-19症例は男性よりも女性が多かった(Table 1)。併存疾患あり or 医薬品使用歴ありの患者の割合の範囲は、24%(CPRD Aurum)から44%(LPD)であった。COVID-19入院患者では(Table 1)、
- 年齢中央値: 67歳
- 性別: 大半が男性
- 併存疾患あり or 医薬品使用歴あり: 72%(32,329名中23,271名)
という結果であった。各データベースにおける最後のindex dateの範囲は、2021年1/30(CPRD Aurum)から2021年7/31(LPD)だった。
VTEの90日間累積発症率の範囲は0.21%(95%CI: 0.16~0.27; IPCI)から0.89%(95%CI: 0.77~0.83; SIDIAP CMBD-AH)であり, 入院患者で4.52%(95%CI: 4.37~4.68)とより高値だった。ATEの90日間累積発症率の範囲は0.06%(95%CI: 0.05~0.07; CPRD Aurum), 0.06%(95%CI: 0.04~0.11; LPD)から0.79%(95%CI: 0.77~0.82; SIDIAP CMBD-AH)であり, 入院患者で3.08%(95%CI: 2.96~3.21)へ上昇していた。しかしながら、COVID-19症例の90日間致死率の範囲は1.08%(95%CI: 0.96~1.20; IPCI)から1.99%(95%CI: 1.95~2.03; SIDIAP CMBD-AH)であった。入院患者では、致死率は14.61%(95%CI: 14.22~15.00)へ上昇した。
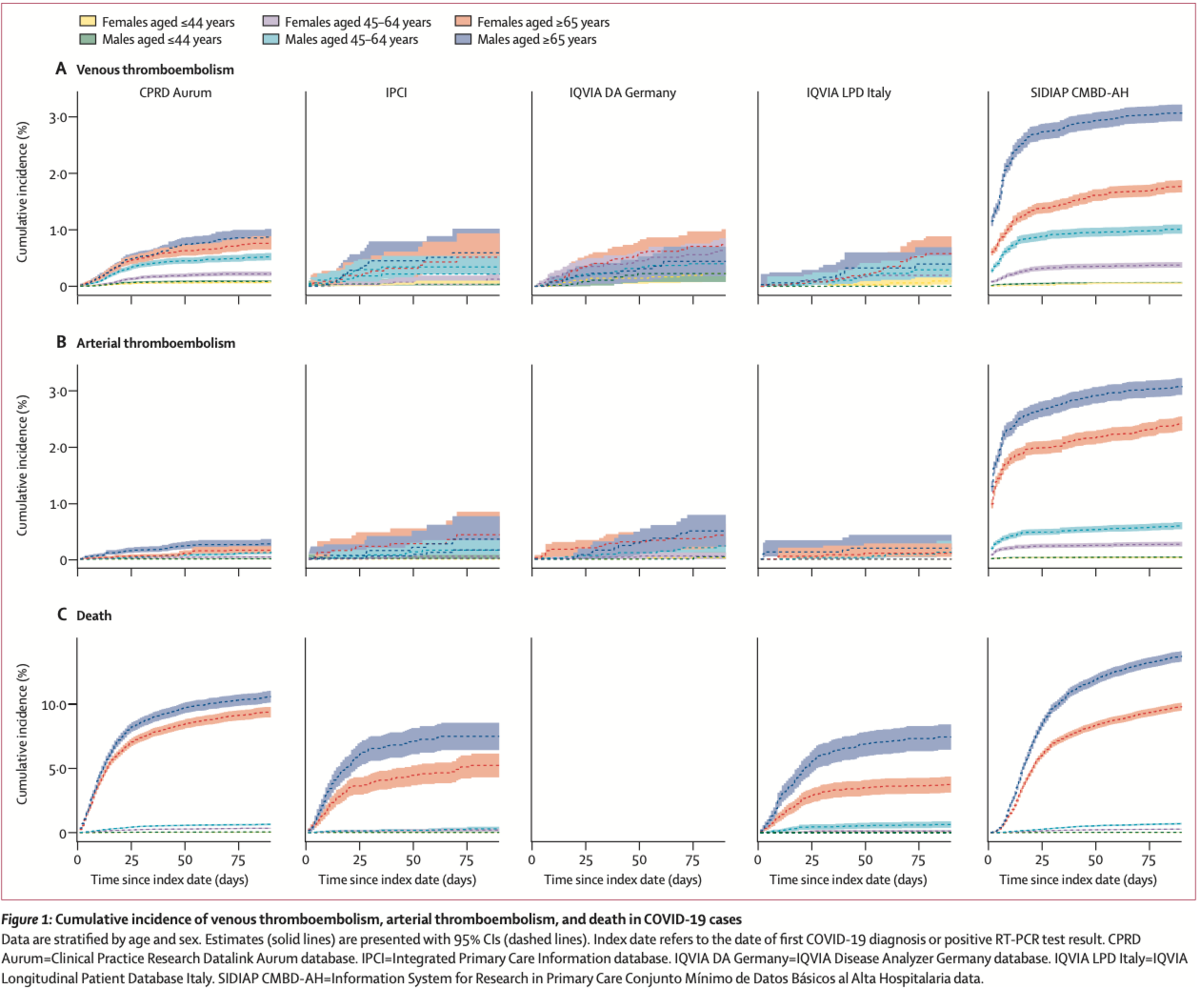
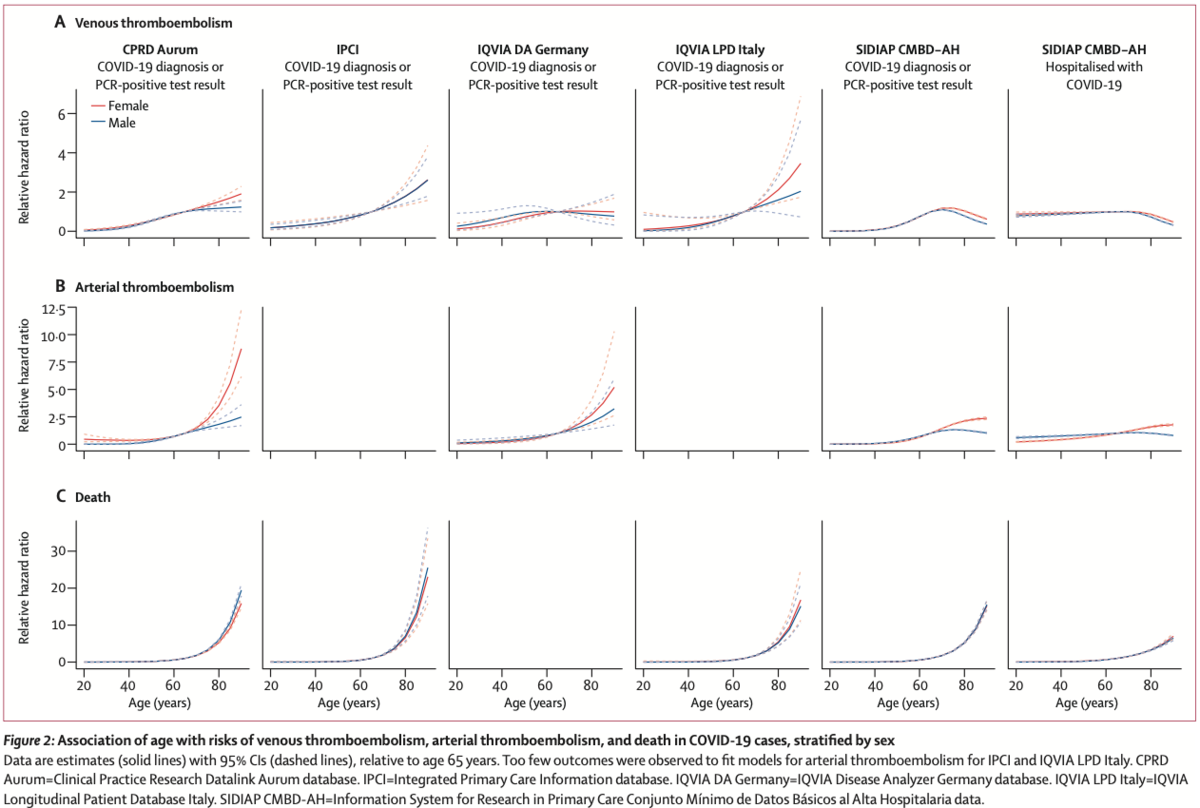
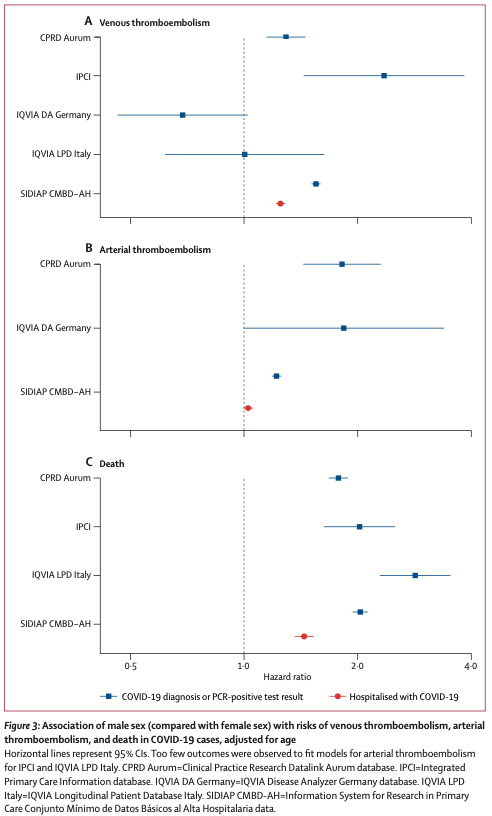
VTE・ATE・死亡の発症率は65歳以上で高かった(Figure 1)。COVID-19入院患者において、高齢によりATE・死亡のリスクは増加したが、VTEでこうしたパターンは見られなかった。年齢のみを変量としたモデルでは、死者を収集したデータベース全てにおいて、最も高齢な集団で死亡リスクが最も高かった(Figure 2)。同様にして、年齢が上昇するにつれてATEリスクは増加したものの、この増加は死亡リスクの増加ほどではなかった。VTEリスクは年齢上昇とともに増加したものの、一部のデータベースでは70歳あたりで平坦化または低下した。年齢によって調整したモデルでは、全てのデータベースにおいて、男性がATE・死亡リスク増加と関連していた(Figure 3)。CPRD Aurum, IPCI, SIDIAP CMBD-AHでは女性よりも男性でVTEリスクが高かったが、DAとLPDではそうならなかった(Figure 3)。
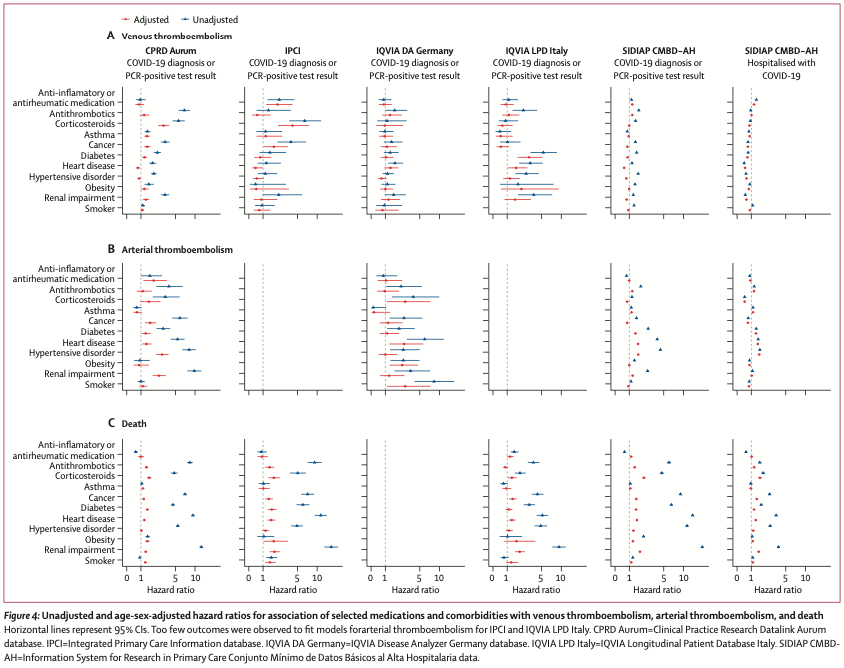
未調整モデルでは、大半の医薬品使用歴と併存疾患がVTE・ATE・死亡リスク上昇と関連していた(Figure 4)。しかし年齢・性別で調整すると、これらの関連性の大半が弱まった(Figure 4)。ATEについては、心疾患または高血圧の既往のある患者で一貫してリスクの上昇が見られた。死亡リスクに関しては一貫して関連性が見られた: ステロイド, 糖尿病, 腎疾患は死亡率上昇と関連していた。
外来でのVTEは転帰悪化と関連しており、年齢調整hazard ratio(HR)は
- 入院のHR: 1.36(95%CI: 0.95~1.96)
- 入院せずに死亡するHR: 4.42(95%CI: 3.07~6.36)
だった。入院後のVTEは死亡リスク増加とも関連していた(HR: 1.63[95%CI: 1.39~1.90])。外来でのATEは入院せずに死亡するリスク増加と関連(HR: 3.16[95%CI: 2.65~3.75])していたが、入院リスク増加と関連はしていなかった(HR: 1.05[95%CI: 0.89~1.25])。同様にして、入院後のATEは死亡の調整後HR 1.93(95%CI: 1.57~2.37)と関連していた。
(4) 考察
PCRで陽性またはCOVID-19と診断された患者において、
- VTEの90日間累積発症率は0.2~0.8%
- ATEの90日間累積発症率は01.~0.8%
だった。患者レベルのデータが入院中経過とリンクされているデータベースでは、
- COVID-19入院患者のVTEの90日間累積発症率は4.5%まで増加
- COVID-19入院患者のATEの累積発症率は3.1%まで増加
していた。90日間致死率は、
- COVID-19症例で1.1~2.0%
- 入院患者で14.6%
だった。
最高齢の患者において致死率がかなり高くなるにも関わらず、年齢上昇に伴うATEリスク増加はそこまで顕著ではなく, またVTEリスクは一部のデータベースで70歳あたりでピークとなっていたように見えた。年齢で調整後、男性はVTE・ATE・死亡リスク上昇と関連していた。その上、未調整モデルでは複数の併存疾患・医薬品使用歴がVTE・ATE・死亡リスク上昇と関連していたものの、年齢と性別で調整後に関連性は弱まった。
VTE・ATE発症はいずれも、COVID-19関連健康転帰の悪化と関連していた。COVID-19による入院前のVTE発症は入院リスクと入院前死亡リスクの上昇と関連しており, また、入院後のVTE・ATE発症は入院患者致死率上昇とも関連していた。
COVID-19発生より前の過去の研究では、呼吸器感染症罹患後にVTE・ATEリスクが上昇することが示されている。COVID-19罹患時のVTE・ATE有病率を記述する研究は複数行われている; しかし、この研究は主にCOVID-19で入院した患者にフォーカスしており, また、この研究の患者集団ですら、推計値は顕著に開きがあった。まとめると、ICUに入室したCOVID-19患者に限定していない研究では、入院中のVTE有病率は9%, ATE有病率は4%であった(今回の研究における数値は上記の通り)。予想された通りであるが、この研究では、COVID-19患者全体のVTE・ATE発症率/有病率は入院患者の数値よりも低かった。SARS-CoV-2感染者数が膨大であることを考慮すると、こうした比較的小さいリスクに多くの患者が影響されるということを示している。入院中データ(SIDIAP CMBD-AH)とリンクさせた推計値は高値であり、外来診療記録のみに由来するデータでは少なく報告されてしまう可能性が示唆される。また、COVID-19に罹患しているのに医療機関を受診していない人がカバーされていないことも注意が必要である。
今回は久々の?論文紹介だったのですが、毎回すげー冗長になりがちですし, 和訳に難渋したり, 統計学などまだ私が理解できていない概念もありますので、所々割愛していることをどうかご容赦下さい。このデータは欧州のものですし、アジアなどの文化・人種等の背景が違う地域では若干の差が出るかもしれません。また、コロナワクチンを接種したか否か(或いは、接種済みでも1回だけなのか, 2回接種したのか, 3回目・4回目を済ませたのか)により差が出てくる可能性もあるかもなので、そうしたデータも見てみたいものです。いずれにせよ、こうした血栓症のリスクも考えると、COVID-19にはかかりたくないものですね。